Rhumatologie
Polyarthrite rhumatoïde : pourquoi et comment décroître la corticothérapie ?
Dans la polyarthrite rhumatoïde (PR), l’EULAR positionne les corticostéroïdes (CS) comme traitement d’appoint, l’ACR les déconseille si possible. Là où les deux sociétés se rejoignent, c’est sur l’absolue nécessité d’un sevrage à trois mois.
Malgré ces recommandations, 80% des patients sont toujours sous CS à un an, avec les risques intrinsèques. Dans ce contexte, il faut se poser trois questions [1]. Les CS sont-ils nécessaires ? Quels sont les risques ? Comment réaliser le sevrage dans de bonnes conditions ?
Les CS : oui, non, peut-être ?
 L’efficacité a été démontrée dans de nombreuses études. Notamment, NORD STAR (patients naïfs de traitements de fond) a montré la non-infériorité (sur le taux de rémission CDAI) à 24 semaines de l’instauration de méthotrexate (MTX) + CS, vs MTX + certolizumab ou MTX + tocilizumab.
L’efficacité a été démontrée dans de nombreuses études. Notamment, NORD STAR (patients naïfs de traitements de fond) a montré la non-infériorité (sur le taux de rémission CDAI) à 24 semaines de l’instauration de méthotrexate (MTX) + CS, vs MTX + certolizumab ou MTX + tocilizumab.
La non-infériorité n’était pas obtenue vs MTX + abatacept. Dans le groupe MTX + CS, la dose de CS était de 20 mg/j, réduite jusqu’à 5 mg/j à neuf semaines puis arrêtée. L’objectif n’était pas de promouvoir les CS ou une biothérapie en première intention, mais de montrer que les CS font aussi bien qu’une biothérapie d’emblée dans une PR récente.
De quels risques parle-t-on ?
Le risque infectieux est une augmentation de 30% du risque d’hospitalisation pour une dose < 5 mg/j et fois deux pour une prise entre 5 et 10 mg/j chez 216.000 patients avec une PR suivis pendant un an [2].
Le risque cardiovasculaire (composite du premier infarctus du myocarde ou AVC) est confirmé (HR = 1,5), quelle que soit la dose de GC (< 5 mg/j, 5 à 10 mg/j, ou > 10 mg/j).
Le risque de mortalité dans le registre RABBIT est plus élevé chez les patients traités par CS à une dose > 5 mg/j vs < 5 mg/j avec un effet dose dépendant qui n’est pas lié à l’activité de la maladie.
Comment décroître les CS ?
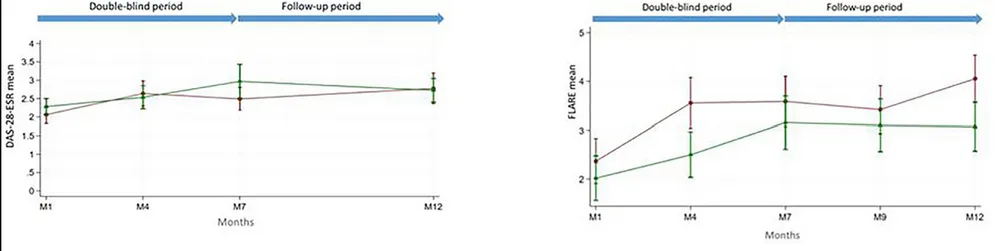
Dans l’étude STAR [3] (maladie de faible activité sous traitement de fond et CS à 5 mg/j avec une dose stable > trois mois), une diminution de 1 mg / mois jusqu’à l’arrêt est équivalente à un relais par hydrocortisone 20 mg/j puis 10 mg/j, puis arrêt à sept mois (47% vs 55%, p = 0,4). Aucun cas d’insuffisance surrénalienne n’a été rapporté.
Les recommandations ESE [4] proposent deux stratégies sans privilégier l’une ou l’autre : décroître progressivement les CS sans bilan ou en dosant le cortisol à 8h. La diminution est poursuivie si le résultat est > 10 μg/dl (300 nmol/l), une substitution doit être débutée si le résultat est < 10 μg/dl.
Quatre messages
- Les CS sont envisageables dans l’espoir de pouvoir les arrêter après trois à six mois.
- Une corticothérapie au long cours même à faible dose (5 mg/j) augmente les risques infectieux et cardiovasculaires et la mortalité.
- Les recommandations proposent une diminution guidée ou non par un dosage du cortisol à 8h.
- Le risque de poussée articulaire existe sous dose diminuée, mais la balance bénéfice-risque est en faveur de la diminution et si possible de l’arrêt des CS [5].
Références
1. Forien M. Journées Viggo-Petersen 2026
2. George MD, et al. Risk for Serious Infection With Low-Dose Glucocorticoids in Patients With Rheumatoid Arthritis : A Cohort Study. Ann Intern Med 2020; 173: 870-8
3. Ruyssen-Witrand A, et al. Comparison of two strategies of glucocorticoid withdrawal in patients with rheumatoid arthritis in low disease activity (STAR): a randomised, placebo- controlled, double-blind trial. Ann Rheum Dis 2025; 84: 49-59
4. Beuschlein F, et al. ESE guidelines. Eur J of Endocrinology 2024;190:G25-G51. https://doi.org/10.1093/ejendo/lvae029
5. Burmester GR, et al. Continuing versus tapering glucocorticoids after achievement of low disease activity or remission in rheumatoid arthritis (SEMIRA): a double-blind, multicentre, randomised controlled trial. Lancet 2020;396(10246):267‑76
